Yuanfeng POV: Bijgewerkte EUDAMED-tijdlijn
De EU-Commissie heeft onlangs updates aangekondigd voor de voltooiing en uitvoering van EUDAMED op basis van wijziging 2024/1860.Dit artikel geeft een overzicht van de huidige EUDAMED-tijdschema's en ons standpunt over deze tijdschema's om de industrie te helpen zich daarop voor te bereiden..
Huidige EUDAMED-tijdlijnen:
- De doeldatum voor de eerste verplichte toepassing van functionele EUDAMED-modules is nog steeds 1 januari 2026.De Vigilance-module zal naar verwachting vanaf het derde kwartaal van 2026 verplicht zijn en de volledige EUDAMED-functionaliteit is gepland voor het tweede kwartaal van 2027..
- De modules Actor, UDI & Devices, Certificates en Market Surveillance worden momenteel gecontroleerd.De onafhankelijke MVP-audit is bedoeld om de functionaliteit en interconnectiviteit van de modules die als auditklaar worden beschouwd, te beoordelen en te bevestigen.Deze audit zal naar verwachting in het tweede kwartaal van 2025 zijn afgerond.
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)De Actor, UDI & Devices, Certificaten en Market Surveillance-modules zullen naar verwachting eind tweede kwartaal 2025 volledig functioneren, wat leidt tot de verplichte toepassingsdatum van 1 januari. 2026.
- Ik weet het niet. - De Actor-, UDI & Devices-, Certificaten en Market Surveillance-modules zullen naar verwachting eind tweede kwartaal 2025 volledig functioneren en op 1 januari 2026 verplicht zijn voor gebruik in de industrie.
- De Vigilance-module maakt geen deel uit van de lopende MVP-audit en zal niet volledig functioneel worden verklaard samen met de eerder genoemde modules.De herziene tijdschema geeft aan dat de audit van die module plaatsvindt tussen het tweede en derde kwartaal van 2025, met als doel de verplichte toepassingsdatum in het tweede kwartaal van 2026.
- Ik weet het niet. - De ontwikkeling van de module Klinisch onderzoek/prestatieonderzoek (CI/PS) is van plan door te gaan tot het derde kwartaal van 2026.Een audit om de module CI/PS samen met de andere vijf (5) modules te beoordelen zal worden afgerond zodra de MVP van de CI/PS is ontwikkeld..
- Ik weet het niet.
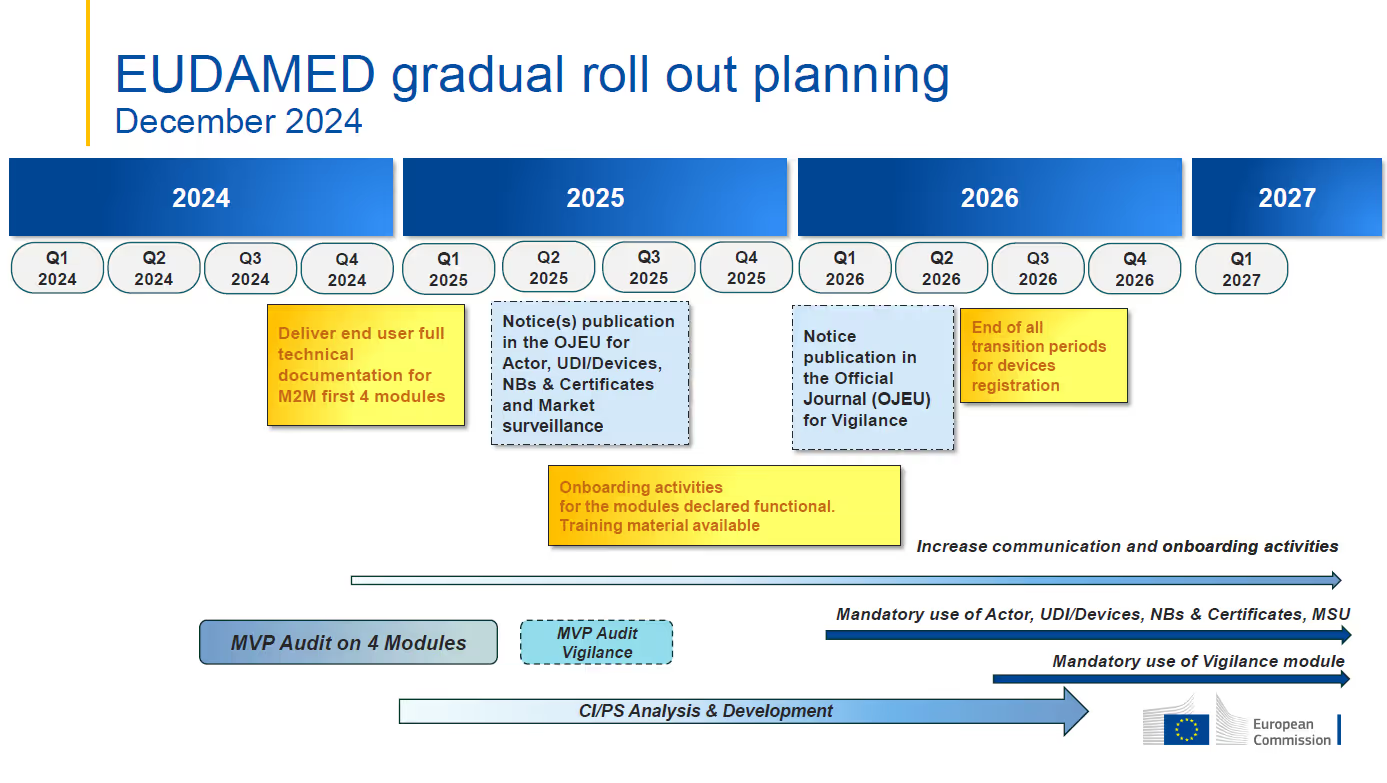
Foto met toestemming van deEuropese Commissie
De EU-Commissie heeft onlangs updates aangekondigd voor de voltooiing en tenuitvoerlegging van EUDAMED op basis van:wijziging 2024/1860.Dit artikel geeft een overzicht van de huidige EUDAMED-tijdschema's en ons standpunt over deze tijdschema's om de industrie te helpen zich daarop voor te bereiden.
Huidige EUDAMED-tijdlijnen:
- De doeldatum voor de eerste verplichte toepassing van functionele EUDAMED-modules is nog steeds 1 januari 2026.De Vigilance-module zal naar verwachting vanaf het derde kwartaal van 2026 verplicht zijn en de volledige EUDAMED-functionaliteit is gepland voor het tweede kwartaal van 2027..
- De modules Actor, UDI & Devices, Certificates en Market Surveillance worden momenteel gecontroleerd.De onafhankelijke MVP-audit is bedoeld om de functionaliteit en interconnectiviteit van de modules die als auditklaar worden beschouwd, te beoordelen en te bevestigen.Deze audit zal naar verwachting in het tweede kwartaal van 2025 zijn afgerond.
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)De Actor, UDI & Devices, Certificaten en Market Surveillance-modules zullen naar verwachting eind tweede kwartaal 2025 volledig functioneren, wat leidt tot de verplichte toepassingsdatum van 1 januari. 2026.
- Ik weet het niet. - De Actor-, UDI & Devices-, Certificaten en Market Surveillance-modules zullen naar verwachting eind tweede kwartaal 2025 volledig functioneren en op 1 januari 2026 verplicht zijn voor gebruik in de industrie.
- De Vigilance-module maakt geen deel uit van de lopende MVP-audit en zal niet volledig functioneel worden verklaard samen met de eerder genoemde modules.De herziene tijdschema geeft aan dat de audit van die module plaatsvindt tussen het tweede en derde kwartaal van 2025, met als doel de verplichte toepassingsdatum in het tweede kwartaal van 2026.
- Ik weet het niet. - De ontwikkeling van de module Klinisch onderzoek/prestatieonderzoek (CI/PS) is van plan door te gaan tot het derde kwartaal van 2026.Een audit om de module CI/PS samen met de andere vijf (5) modules te beoordelen zal worden afgerond zodra de MVP van de CI/PS is ontwikkeld..
- Ik weet het niet.

Foto met toestemming van deEuropese Commissie
Rimsys ziet de impact van deze aankondiging voor elke belanghebbende groep als volgt:
Yuanfeng
UDI is vooropgesteld, evenals toekomstige interactie met de Vigilance module.Rimsys zal de UDI-functionaliteit en de functionaliteit van het markttoezicht na de datum van de herziening blijven ontwikkelen, ongeacht de bijgewerkte streefdatumsWij erkennen ook de potentiële impact van het opzetten van gegevensoverdracht (DTX) -mogelijkheden om met EUDAMED te communiceren in een machine-to-machine (M2M) -capaciteit.Met de publicatie van de definitieve vereisten voor M2M DTX aan EUDAMED, Rimsys is in de positie om onze verbinding af te ronden en M2M-mogelijkheden te leveren als onderdeel van de EUDAMED-oplossing.
Industrie/klant
Aangezien de Europese Commissie de EUDAMED-termijnen herhaaldelijk heeft bijgewerkt, verwachten wij dat de industrie een zekere terughoudendheid zal hebben om de nieuwe streefdatums te aanvaarden.Dit kan de hervatting van de EUDAMED-voorbereidingen vertragen.Wij verwachten echter niet dat de EG deze bijgewerkte tijdschema's zal verleggen.Fabrikanten die geen plan hebben om gegevens voor het tweede kwartaal van dit jaar aan EUDAMED in te dienen, moeten verwachten dat zij aanzienlijke uitdagingen zullen ondervinden om aan deze termijnen te voldoen.Met de audit van de verwachte modules in gang met de bijbehorende gepubliceerde technische documentatie,Rimsys beveelt aan nu maatregelen te nemen om de regelgevende gegevens te organiseren en hun informatie vroegtijdig in te dienen bij alle beschikbare EUDAMED-modules.
EU-Commissie
De Commissie beveelt de industrie ten zeerste aan haar oplossing te blijven ontwikkelen en gegevens op vrijwillige basis in te dienen.De Commissie is van mening dat het vroegtijdig indienen van gegevens bedrijven een voordeel zal geven door hun gegevens voor de hele wereldwijde MedTech-industrie te hebben.Deze bedrijven zullen ook in de eerste rij staan om met de middelen van de Commissie te werken als er problemen met de indiening van gegevens optreden.
* Opmerking: dit artikel omvat interpretaties en adviezen van de regelgevende instanties van de Lid-Staten.YuanfengWij proberen zo informatief mogelijk te zijn, maar deze informatie is niet bedoeld om de officiële richtlijnen van de regelgevende instanties te vervangen.

